據港交所10月3日披露,江蘇荃信生物醫藥股份有限公司–B(荃信生物)向港交所主板提交上市申請,中金公司爲其獨家保薦人。據悉,該公司曾於2023年3月31日向港交所主板遞交過上市申請。

招股書顯示,荃信生物是一家完全專注於針對自身免疫及過敏性疾病生物療法的臨牀階段生物科技公司。該司有兩個核心產品QX002N及QX005N,均是自行开發。QX002N是一種處於III期臨牀試驗的IL-17A抑制劑,治療強直性嵴柱炎(AS)療效良好。QX005N則是一種阻斷IL-4R的單克隆抗體(mAb),而IL-4R是一種針對廣泛適應症進行研究的經驗證靶點。
荃信生物已在中國啓動QX005N用於特應性皮炎(AD)、結節性癢疹(PN)及慢性鼻竇炎合並鼻息肉(CRSwNP)的II期臨牀試驗。截至最後實際可行日期(指2023年9月23日),公司就核心產品有19項專利及專利申請。截至同日,除核心產品外,荃信生物還有其他七種管线候選藥物,其中四種處於臨牀階段。公司的產品管线涵蓋了在中國自身免疫和過敏性疾病有明顯醫療需求的四個主要領域,即皮膚、風溼、呼吸道及消化道疾病。
市場格局方面,根據弗若斯特沙利文的資料,於2022年,中國的AS患者人數爲390萬人,估計於2030年將達到400萬人。於2022年,中國AS藥物市場規模爲18億美元,預計到2030年將達到65億美元,復合年增長率爲17.4%。QX002N獲得批准及商業化後,荃信生物預期,QX002N將面臨跨國制藥公司獲批生物藥物的激烈競爭以及在中國用於AS的臨牀开發候選藥物的潛在競爭。
荃信生物提到,截至最後實際可行日期,該等藥物及候選藥物全爲TNF抑制劑及IL-17抑制劑。TNF抑制劑包括阿達木單抗及多種阿達木單抗生物類似藥及擬定生物類似藥。截至最後實際可行日期,中國有兩種IL-17A抗體藥物(即司庫奇尤單抗及依奇珠單抗)獲批准用於治療AS,兩者亦已獲FDA批准。截至同日,除荃信生物的QX002N外,中國還有九種處於臨牀階段適用於AS靶向IL-17的候選生物藥物。
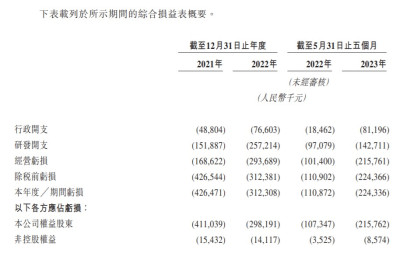
財務方面,公司於2021年、2022年未有營業收入,相應的研發开支分別爲1.52億、2.57億元人民幣,相應的淨虧損分別爲4.26億、3.12億元人民幣。
據荃信生物在招股書中所述,公司很大程度上依賴候選藥物的成功(公司的所有候選藥物均處於臨牀前或臨牀开發階段)。倘公司無法成功完成臨牀开發候選藥物,或上述事項遭遇重大推遲,該司的業務前景將嚴重受損。
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:新股消息 | 荃信生物二次遞表港交所 主攻自免及過敏性疾病領域
地址:https://www.breakthing.com/post/101201.html







