對於創新藥而言,臨牀研發進展無疑是股價的最好的催化劑。
在ESMO大會上,加科思-B(01167)以口頭報告形式公布自主研發的格來雷塞(KRAS G12C抑制劑)與JAB-3312(SHP2抑制劑)聯合療法臨牀數據。臨牀試驗結果驗證了格來雷塞與JAB-3312聯合療法的安全性及有效性,爲進一步的注冊臨牀試驗奠定了基礎。
受此消息的影響,10月24日,加科思股價大漲19.21%,不過次日並沒有延續大漲的行情,而是衝高回落,截至收盤時間,公司股價跌4.27%,報4.04港元/股,成交額4007萬港元。

(行情來源:智通財經)
就數據來說,加科思此次在ESMO會上公布的數據確實亮眼,有效性方面,在所有劑量組的晚期非小細胞肺癌,KRAS G12C抑制劑與SHP2抑制劑兩藥聯合一线治療的ORR爲65.5%(38/58),DCR爲100%。其中在800毫克格來雷塞(每日給藥一次)及2毫克JAB-3312(給藥一周間歇一周)聯用的劑量組中,客觀緩解率爲86.7%(13/15),DCR爲100%。
安全性方面,在所有劑量組中,三級和四級TRAE(治療相關不良事件)的發生率爲39.6%,而800毫克格來雷塞及2毫克JAB-3312聯用的劑量組中,三級和四級的TRAE發生率36.7%。
數據優異,但股價卻並沒有持續走強,背後的原因或爲加科思要將其變現難度不小,並且加科思的SHP2被艾伯維退貨過。
SHP2聯用大勢所趨
過去幾十年,SHP2一直被認爲是“不可成藥”靶點。但隨着近年來的研究進展,SHP2靶向藥研發逐漸取得突破,使得它成爲當下新藥研發的前沿靶點之一,並有望與包括免疫檢查點藥物在內的多種藥物聯合使用來提高腫瘤治療的效果。如今,SHP2作爲一個明星癌症靶點,已吸引了國內外多家藥企布局研發,如諾華、艾伯維、輝瑞、加科思、諾誠健華和蘇州勤浩醫藥等。
但目前全球範圍內針對SHP2靶點尚無藥物獲批上市,不過有多款SHP2抑制劑獲批臨牀。其中,進展最快的處於2期臨牀階段的藥物TNO-155,這款產品也是首款進入臨牀階段的SHP2抑制劑。
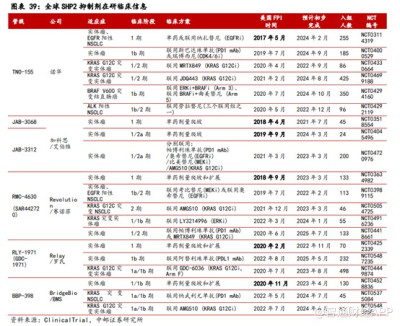
不過,諾華在SHP2抑制劑的研發上並不順利,其中表現在SHP2抑制劑的單藥效果不佳。在2021年ASCO年會上,諾華公布報告了TNO155在成年晚期實體瘤患者中的一期臨牀試驗初步結果。結果顯示,截至2021年2月8日,在入組的125名患者中,客觀緩解率爲0%,更是有94%的患者因爲疾病進展、不良反應、死亡而停止了治療。
也正是因此,後來者幾乎默認了研發SHP2抑制劑主要用在聯合療法上。
不過,安進KRAS G12C抑制劑Lumakras聯合RMC4630並未出現“1+1>2”的效果,加之早在2021年,Revolution就已經停止了RMC-4630與MEK抑制劑的聯藥試驗,這意味着SHP2的聯藥組合或在不斷減少,無疑限制了該靶點產品未來的成長空間。
從聯合療法角度來看,作爲一款輔助用藥,基於SHP2靶點在激活RAS蛋白和執行PD1信號通路上的功能,因此SHP2抑制劑聯合PD(L)1單抗/KRASG12C抑制劑被業界高度認可。中郵證券認爲SHP2抑制劑與 PD(L)1 單抗聯用治療非小細胞肺癌(NSCLC)和食管鱗癌(ESCC)兩個主要適應症。參考JNCC數據,2021年中國新發NSCLC和ESCC數量分別爲74.0萬和25.2萬,適用於SHP2i聯用PD(L)1的2L驅動基因陰性晚期NSCLC和2L晚期 ESCC患者數量分別爲16.6萬和10.6萬人,合計27.2萬人。按20%滲透率,年費用10萬元計算,SHP2抑制劑在三個主要適應症的潛在市場爲54.4億元。
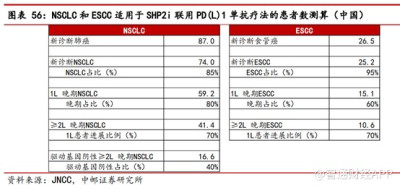
也就是說,若一家藥企要推動SHP2抑制劑上市,並且佔有這巨大的市場,基本上只能綁定PD-1和KRAS抑制劑。
而艾伯維之所以將加科思的SHP2抑制劑退貨,並非其臨牀數據表現不佳,或與艾伯維自身研發管线有關。據艾伯維發布的2022年財報來看,艾伯維的業務主要分爲免疫、血液腫瘤、神經、醫美、眼科、女性保健和其他業務七個板塊,其中自身免疫疾病的份額仍接近半壁江山,其次是血液腫瘤業務。
其研發管线既沒有PD-1也沒有KRAS,也就是說,引進SHP2抑制劑,對於艾伯維而言並沒有太大的好處,也很難獲得可觀的商業價值,基於此,加科思的SHP2被艾伯維退貨也在所難免。
現如今加科思自己聯用KRAS,並且數據表現不錯,加上其核心產品格來雷塞即將步入商業化,自主商業化在所難免。那么加科思目前商業化進展又如何呢?
自主商業化剛起步
從研發管线角度來看,格來雷塞是加科思研發進展最快的產品。目前格來雷塞3項適應症均在推進中,其中針對非小細胞肺癌這一適應症中國關鍵注冊臨牀預計今年9月完成入組,2024H1提交NDA申請,進度依然保持國內前三;聯用利妥昔單抗治療後线CRC數據於JCA-AACR 2023發表,進度國內第一,ORR 62.8%優於海外競品,PFS數據值得關注;今年8月獲CDE授予治療2L+胰腺癌的突破性療法認定,預計今年9月啓動中國關鍵注冊臨牀,胰腺癌早期數據預計將在2024年1月的ASCO GI發表。

也就是說,距離加科思正式進入“造血時代”還有1年不到的時間。而其能商業化成功與否,一方面是核心產品格來雷塞再市場的競爭力,另一方面是加科思自身商業化布局能力。
就產品而言,據了解,在藥物的有效性和安全性上,格來雷塞的ORR爲53.3%,DCR接近100%。從藥物的作用機理來看,加科思把部分化合物做成偏鹼的分子,因此讓KRAS G12C對胃腸的損傷非常小,胃腸道毒性明顯低於競品。從安全性數據上看,加科思和安進數據接近,但在“任意副作用造成試驗中斷”這一指標上,安進發生率爲4%,加科思爲0。
從競爭角度來看,全球處於臨牀階段的KRAS G12C抑制劑共25款,其中批准上市2款,III期臨牀2款,II/III期臨牀1款,II期臨牀3款,I/II期臨牀7款,I期臨牀10款。中國處於臨牀階段的KRAS G12C 抑制劑共18款,III期臨牀3款,II/III期臨牀1款,II期臨牀2款,I/II期臨牀6款,I期臨牀6款。
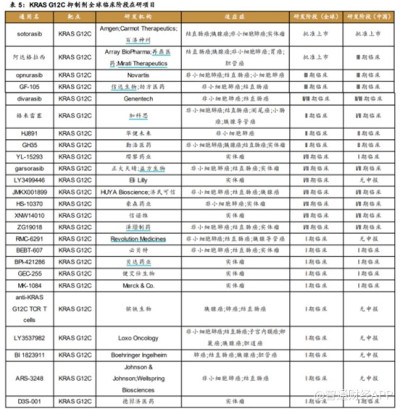
從臨牀進展來看,除了百濟、再鼎和信達外,加科思是國內在研企業中進展較快的,但適應症基本上大同小異,因此,待加科思產品上市後,並不具備市場先發優勢。
除此之外,加科思的財報亦不容樂觀,據其2023年上半年財報顯示,加科思上半年收入4030萬元,均來自艾伯維籤訂的研發、制造及商業化SHP2抑制劑的許可及合作協議所產生的研發成本報銷,期內公司虧損1.66億元,現金及現金等價物約爲7.84億元,較2022年同期減少約6.75億元。原本還有艾伯維的裏程碑收入,現如今,其SHP2抑制劑被艾伯維退貨,這在一定程度上影響了加科思的現金情況。
一年燒近7億,這也是說未來一年內,加科思產品再不上市銷售,其現金流也將岌岌可危。爲了減少生產成本,生產方面,加科思正在申請上市許可持有人(MAH)資格,公司將與一家CDMO企業合作,遵循MAH系統進行生產。
銷售方面,公司也在積極組建營銷團隊,建立自己的中央營銷部門,促進學術交流和市場准入。目前來看,加科思的商業化體系正开始組建,但因其核心產品市場競爭相對較爲激烈,其商業化道路能否順利尚不明朗。
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:加科思-B(01167):拼命的關鍵年?
地址:https://www.breakthing.com/post/105823.html







