
日前,健世科技向港交所遞交招股書,擬在香港主板掛牌上市。健世科技是一家致力於提供結構性心髒病領域創新解決方案的高科技醫療器械企業,开發出針對不同類型結構性心髒病的一系列治療解決方案。結構性心髒病市場需求龐大,但是由於供給不足,存在較大的需求缺口,健世科技的創新解決方案將有力地填補結構性心髒病治療的各個市場缺口。
健世科技主打的兩款核心產品是LuX-Valve和Ken-Valve,此外還有8款具備領先技術的在研產品,針對不同類型瓣膜疾病及心力衰竭。LuX-Valve、Ken-Valve,還有LuX-Valve的新一代產品LuX-Valve Plus都已經進入確證性臨牀試驗階段,根據公司的預期,LuX-Valve將在明年下半年實現商業化,而Ken-Valve將在2024年上半年實現商業化。而截至最新時間,LuX-Valve的新一代產品LuX-Valve Plus也已經完成可行性臨牀試驗階段,進入到了確證性臨牀試驗階段。全球共三款進入到確證性臨牀階段的三尖瓣置換產品,其中健世科技自主研發的產品佔兩席。
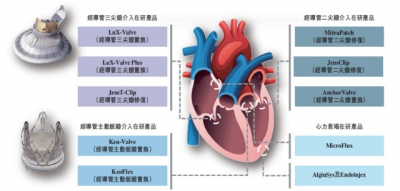
經導管三尖瓣介入產品
LuX-Valve是公司自主研發的第一代經導管三尖瓣置換系統,專爲重度三尖瓣返流及高手術風險患者設計。2019年1月,LuX-Valve獲國家藥監局納入創新醫療器械特別審查通道(「綠色通道」),因此獲准了快速審評審批資格。2022年2月,公司完成了LuX-Valve確證性臨牀試驗6個月的隨訪,已經在2022年8月完成1年的確證臨牀試驗隨訪。公司預計2023年下半年LuX-Valve有望獲得國家藥監局的商業化批准。LuX-Valve是世界首款完成確證性臨牀試驗受試者入組的在研產品,有望成爲全球首批獲准商業化的經導管三尖瓣置換產品之一。
LuX-Valve在三尖瓣返流治療中處於什么地位呢?2021年,全球中度至重度三尖瓣返流患者數量達到5170萬人,而且隨着老齡化的嚴重,患者數量還會持續增加,到2030年預計達到6070萬人,可以說三尖瓣反流市場具有非常大的需求空間。通常三尖瓣返流患者一般生活質量低,且死亡率高(約36%的重度三尖瓣返流患者在確診後一年內去世,約47.8%在確診後五年內去世),對治療有強勁需求。預計到2030年,在中國進行的三尖瓣疾病介入治療將達到約200,900例,相較於主動脈瓣疾病手術的109,500例和二尖瓣疾病手術的54,100例則市場空間更大。中度至重度三尖瓣返流的常規療法包括藥物治療和外科三尖瓣介入,但是前者效果不佳,後者局限性比較大,對於重度、老齡患者的可行性比較差,而經導管三尖瓣介入療法的侵入小、痛苦少、恢復快,優勢非常明顯,所以,經導管三尖瓣介入療法會越來越流行。
目前,全球還沒有商業化的經導管三尖瓣置換產品。LuX-Valve是世界首款完成確證性臨牀試驗受試者入組的在研產品,進入《2021歐洲心髒病學會/歐洲心胸外科協會瓣膜性心髒病管理指南》,進入NMPA創新醫療器械特別審查程序,獲美國食品及藥物管理局突破性醫療器械認定,爲心髒瓣膜疾病治療領域首款獲此認定的國內自主研發醫療器械,LuX-Valve有望成爲全球首批獲准商業化的經導管三尖瓣置換產品之一。而在同類產品中,全球共有三款處於確證性臨牀試驗階段,而國內僅有兩款處於確證性臨牀階段,分別是LuX-Valve、LuX-Valve Plus其中LuX-Valve Plus又是LuX-Valve的新一代產品,所以說,國內市場僅有健世科技一家。

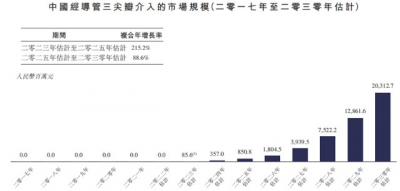
根據行業預測,預計到2030年,國內將會有20萬名患者接受經導管三尖瓣介入手術,市場規模將達到203億,實現從無到有的大幅攀升。健世科技的LuX-Valve有望在其中貢獻多數的增長。除了LuX-Valve,健世科技還在研發它的新一代產品LuX-Valve Plus,LuX-Valve Plus,其受試者入組已於2022年8月完成,並且在9月完成了可行性臨牀試驗的一個月隨訪,預計於2024年上半年商業化。此外,在加拿大聖保羅醫院(St. Paul’s Hospital)成功對11名受試者進行LuX-Valve Plus植入手術,又分別於2022年7月和9月在歐洲於法國和德國成功進行LuX-Valve Plus植入手術,公司預計不久將來會在美國、法國及西班牙等國家進行更多植入手術,造福全球三尖瓣返流患者。此外,公司亦有一款經導管三尖瓣修復夾持系統JensT-Clip。
經導管主動脈瓣介入產品
Ken-Valve是針對主動脈瓣返流的經導管主動脈瓣置換產品。經導管主動脈瓣置換市場目前已經出現了較多的產品,但是絕大多數僅對應主動脈瓣狹窄適應症,並沒有包括主動脈瓣返流適應症。
而全球2021年有2750萬的主動脈瓣返流患者,而且75%初步診斷爲主動脈瓣狹窄的患者同時患有一定程度的主動脈瓣返流。這部分患者的治療需求難以獲得滿足。因此,健世科技自主研發了針對主動脈瓣返流(或兼並狹窄)的經導管主動脈瓣置換產品Ken-Valve,將爲主動脈瓣返流患者提供治療選擇。
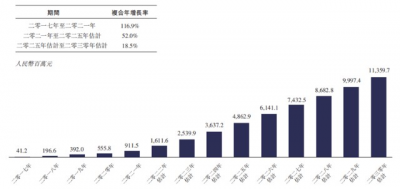
經導管主動脈瓣置換產品跟傳統外科手術相比,與經導管三尖瓣介入療法的優勢相似,也是侵入小、痛苦少、恢復快,經導管主動脈瓣置換產品(尤其是針對主動脈瓣反流的產品)具有巨大的發展空間。根據行業預測,到2030年,全國經導管主動脈瓣置換手術數量將達到10.95萬例,規模將達到113.6億元。盡管相比經導管三尖瓣介入療法的數量和規模偏小,但是同樣也是處於快速增長的階段,其中健世科技的競爭格局也十分強勁,健世科技的Ken-Valve將在2024年上半年實現商業化,成爲國內第二款治療重度主動脈瓣返流的經導管主動脈瓣置換產品。此外,公司也开發了二代產品KenFlex,預計是在今年三季度進行可行性臨牀試驗。
經導管二尖瓣介入產品
公司目前有三款經導管二尖瓣介入產品,全面覆蓋二尖瓣介入治療的多種技術路徑。JensClip是經導管二尖瓣修復夾持系統,具備先進的鎖定機制,在2022年8月進入可行性臨牀試驗。另一款經導管二尖瓣修復系統MitraPatch將在2023年第二季度進入可行性臨牀試驗。公司還在开發經導管二尖瓣置換系統AnchorValve,目前正處於動物研究階段。
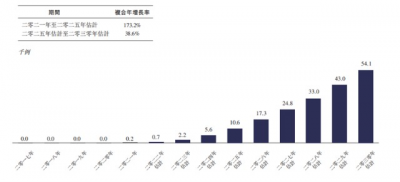
2021年國內進行了200例經導管二尖瓣介入手術,用於治療中度至重度二尖瓣返流,而全國同期有1110萬的中度至重度二尖瓣返流患者,經導管二尖瓣介入手術的潛在需求非常大,弗若斯特沙利文預計到2025年經導管二尖瓣介入手術的數量將達到10600例,到2030年將達到5.41萬例,市場規模也將達到89.4億元。
治療心力衰竭的產品
因爲大部分結構性心髒病到了終末期均會引發心力衰竭,心衰被稱爲是結構性心髒病領域的最後一片战場,健世科技很早便战略性地在心衰領域進行布局,开發多套用於治療心力衰竭的創新醫療器械。公司的房間隔造孔支架及輸送系統MicroFlux主要針對射血分數保留型或輕度降低型心力衰竭,預計2022年第四季度啓動可行性臨牀試驗,心肌填充水凝膠在研產品及其注入器械AlginSys及EndoInjex主要針對射血分數降低型心力衰竭,目前正處於動物研究階段。
目前,藥物是心力衰竭的主要療法,但是對於治療中度至重度心力衰竭的效果並不好,心房間隔分流及心肌填充等介入治療方法的效果更好,發展空間很大。現在只有三款心房間隔分流產品獲得CE認證,一款心肌填充產品獲得CE認證,國內的市場還是空白,公司的產品有很大的發展潛力。
通過這一系列的產线布局,公司建立了強大的一站式平台,具有從發現醫療需求到產品开發以至商業化的全周期研發能力。公司研發團隊具備全面的能力,包括生物材料、縫制技術、架構設計及加工技術。配合即將推出的產品,健世科技已於2021年擴大年產能至約4,000至5,000套,並預期繼續擴大年產能,於2024年年底前達到約10,000套
在商業化進展方面,盡管公司目前還沒有商業化產品,但是公司已在中國逾30家主要醫院進行臨牀試驗,同關鍵意見領袖、主要研究者及醫院都建立了牢固的關系,一旦公司產品通過商業化審批,商業化進展將會取得快速的推進。
作爲創新型醫療器械公司,健世科技還獲得了知名投資機構的投資,包括高瓴資本、春華資本、Cormorant、華夏基金、中國人壽保險及中國人民保險等。考慮到公司在醫院端的布局,健世科技的LuX-Valve等產品商業化後也將开啓快速增長的步伐。相對於傳統的“仿制型”醫療器械公司,健世科技的所有產品均是自主研發的創新型產品,具有絕對優勢。而相對於創新醫療器械公司,公司战略性地布局結構性心髒病市場,尤其是三尖瓣返流市場,市場空間大,增長潛力高,同時公司通過多項全球首創技術,在研發進展上處於全球領先地位,具有更大的優勢。隨着商業化在即,健世科技正在陸續擴大產能,並且已經跟醫院建立了合作關系,預計一旦开始商業化,健世科技將獲得爆發式增長。
- 健世科技-B(09877)
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:健世科技赴港上市,LuX-Valve有望成爲全球首批獲批上市的經導管三尖瓣置換產品
地址:https://www.breakthing.com/post/20231.html







