
2023 年 3 月 13 日,輝瑞(Pfizer)宣布將出資約 430 億美元收購 Seagen,豐富其 ADC 研發與產品管线,再次引爆 ADC 藥物研發市場。在這之前,吉利德 210 億美元收購 Immunomedics、默沙東 28 億美元收購 VelosBio、勃林格殷格翰 14.3 億美元收購 NBE Therapeutics……ADC 賽道上 Big Pharma “交易” 屢現,志在這場 ADC “卡位战”中爭得一席之地。
從 ADC 的市場銷售來看:
自 2019 年,全球 ADC 藥物市場進入高速增長階段。
由阿斯利康和第一三共开發的DS-8201於2019年底獲批上市,用了3年時間便邁過 10 億美元大關,而 TDM-1(Trastuzumab-Emtansin ,曲妥珠單抗—美坦新偶聯物)從 2013 年被美國 FDA 批准上市,到銷售額突破 10 億美元,用了近 5 年。
據 Nature 子刊預測,到 2026 年,全球 ADC 藥物市場規模將達到164 億美元,成爲百億美元級別的重磅市場。
火爆的市場背後是制藥人對 ADC 治療藥物的認可、豐富的研發/產品管线的有力支撐。據不完全統計,目前全球在研 ADC 藥物超過 600 個,其中國內有 240 多個;截止到 2022 年底,全球已有 15 款 ADC 藥物獲批上市。ADC 藥物也被認爲是繼 PD-1 之後的下一個“黃金”賽道。
01
70% 以上的藥企選擇外包
基於 ADC 藥物开發的挑战性,對其 CMC 工作,70% 以上的藥企選擇外包。
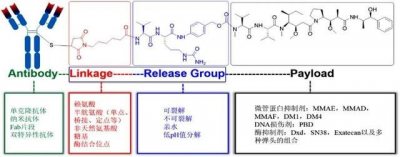
ADC (Antibody-Drug Conjugate),即抗體偶聯藥物,因其精准強效,也被業內稱爲“智能生物導彈”。其包含一個特定靶向抗體(Antibody),能夠精准靶向病變細胞;一個稱爲有效載荷的細胞毒素(Payload),用來加強殺傷腫瘤細胞的能力;還有抗體與 payload 形成的偶聯物。
此組合設計,既可降低脫靶毒性,又能增強對靶細胞及組織的殺死性。與單獨使用抗體或小分子藥物相比,ADC 能幫助實現 1+1>2 的治療優勢。
盡管 ADC 藥物經歷了目前公認的三代變革,技術日臻成熟,但其復雜的結構及對新的靶向分子、payload 及連接子、偶聯方式等的不斷研究改進,致使ADC 藥物在工藝开發與商業化生產等方面更具有挑战性。
靶向分子、payload、靶向分子與 payload 的偶聯,一般需要分別進行工藝开發及生產。
工藝开發過程中需要兼顧不同組分的獨特產品特性,還需要研究偶聯過程中的相互作用及對產品質量的影響,工作復雜且工作量大,大概是傳統大分子藥物研究的 2-3 倍。ADC 藥物的制劑研究也面臨很大的挑战,比如,對於偶聯物,由於 payload 及偶聯方式的不同,改變了靶向大分子的特性,像疏水性、電荷異質等;有些情況下,payload 容易從靶向大分子上脫落下來,造成產品不穩定與用藥時的非特異毒性。
在商業化生產方面,研發企業很難同時兼備靶向大分子、payload 以及偶聯藥原液和制劑的生產能力,如何解決工藝开發和商業化生產的雙重挑战,成爲擺在 ADC 藥物研發企業面前的重大課題。
正是由於 CMC 工作方面的挑战,目前大部分正在研發的 ADC 藥物都在專業的 CRO 或 CDMO 進行 CMC 的工作,據默沙東的 ADC 基地於 2022 年 9 月發布的統計數據顯示,比例超過 70% 。
對於 ADC 藥企來說,選擇與 CDMO 合作,使其提供 ADC 藥物從研發到商業化全流程服務的一站式 CDMO ,在降低風險/成本、縮短周期方面具有更大的優勢。
02
CDMO 競爭格局形成,誰能拔得頭籌?
國內 ADC CDMO 競爭格局已經明朗化,擁有先發優勢的邁百瑞成爲賽道的領跑者之一。
中國率先上市的原創 ADC 藥物——榮昌生物維迪西妥單抗(RC48)的早期臨牀樣品,由邁百瑞提供。2020 年 10 月,邁百瑞 M1 生產設施順利通過了 CDE 對維迪西妥單抗產品上市前的生產現場核查。
截至目前,邁百瑞在全球獲得 40 多個 ADC 綜合項目的合作,已有13 個 ADC 項目獲得臨牀批件。除此之外,邁百瑞每年累計爲客戶提供 400 多個ADC 分子用於體內/體外的藥效評價以及安全性評價等。
創新型研發平台,緊隨行業前沿
自成立起,邁百瑞便布局搭建 ADC 研發平台,目前已擁有新型連接子-毒素的研發設計、偶聯技術的开發與新一代 XDC 候選藥物篩選的技術實力,並已掌握各類成熟的偶聯技術和行業內新興的偶聯技術,例如賴氨酸偶聯、半胱氨酸偶聯、酶催化偶聯、非天然氨基酸偶聯、糖基化位點偶聯等。項目成功率 100%,技術轉移迅速,工藝穩健。
邁百瑞成熟的分析方法开發平台,具有完整的 ADC 藥物分析能力,能夠快速开發出針對 ADC 特異性的分析方法;按照藥典及 ICH 指導原則進行分析方法开發、轉移及確認,具有豐富的方法开發和申報經驗,並持續引進新技術優化平台。
一廠之內,研發+生產
作爲大分子藥物和小分子藥物的結合體,ADC 藥物的开發需要企業同時具備兩方面的能力。如果建立獨立的研發生產設施,按照單品種 2000L 規模計算,抗體、Linker-Payload、ADC 原液、ADC 制劑等GMP 生產設施,投入的費用需要 5 億元左右。
所以,盡管 ADC 研發企業衆多,目前已獨立建廠的卻很少,即使是 CDMO 企業也多選擇投建某一環節,在一廠之內能夠提供 ADC 藥物從研發到生產的企業,在全球範圍內都是少數。
如果一個 ADC 藥物從研發到生產由多個供應商完成,需要進行多次技術轉移,甚至輾轉多地,這必然會導致風險的提高和成本的增加。因此,ADC 藥物开發最佳的選擇就是一廠之內完成研發和生產。
邁百瑞在煙台廠區建成了抗體、Linker-Payload、ADC 原液、ADC 制劑等 GMP 生產設施,可在一個廠區內完成全部 ADC 藥物 CDMO 服務,在降低風險和成本的同時,還可有效縮短項目周期。

邁百瑞 煙台廠區
獨立的 Toxin/Linker-Toxin 合成車間,VC-MMAE 生產規模 200g /批,已獲得 DMF 備案(035537)
已完成四種不同 Linker- Payload 的工藝开發,並且成功從毫克級放大生產至百克級
最大偶聯規模達到 150L,並預留 500L 反應釜工位,充分滿足商業化需求
獨立的 ADC 制劑產线,提供商業化注射劑及凍幹粉針灌裝,可處理 2ml、10ml、20ml、50ml 規格的西林瓶
已完成 100 多批次 ADC 藥物生產,成功率 100%
完善的 GMP/cGMP 質量管理體系,累計接受 100 余次國內外審計和檢查,均順利通過

Toxin/Linker-Toxin 合成車間

凍幹機
定制化服務,提升差異化競爭優勢
ADC 已成爲創新藥產業裏最炙手可熱的細分領域,國內外藥企研發熱情持續高漲,這也意味着競爭會越來越激烈。如何成功完成研發,快速上市,並最大化兌現商業價值,是擺在企業面前的現實問題。
依托於長期的技術與行業經驗積累、全面的平台工藝、商業化生產設施、完善的質量管理體系,邁百瑞已順利完成了 ADC 藥物從研發到生產一體化服務的經驗積累。同時,邁百瑞建立的研發/生產平台在支撐 CDMO 業務運營方面具有技術的共通性,能夠以藥物 CMC 研究階段的任一步驟作爲切入點,滿足不同客戶的差異化需求,最大限度提升產品競爭優勢。
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:ADC 爆火背後超70%外包, 邁百瑞一站式 CDMO 助力藥企佔據先勢
地址:https://www.breakthing.com/post/52662.html







