5月25日,美國食品和藥品管理局(FDA)正式批准輝瑞(NYSE:PFE)的新冠
1年前
5月25日,美國食品和藥品管理局(FDA)正式批准輝瑞(NYSE:PFE)的新冠
5月25日,美國食品和藥品管理局(FDA)正式批准輝瑞(NYSE:PFE)的新冠口服抗病毒藥Paxlovid(奈瑪特韋片/利托那韋片組合)用於治療成人輕度至中度新冠肺炎病症。迄今爲止在美國已开出並用於超過1,160萬例Paxlovid的治療。此前,FDA已在2021年12月對該款藥品授予緊急使用授權,被特別推薦適用於 50 歲以上的和患有基礎疾病的新冠病毒感染者。對於兒童患者,根據現有的緊急授權是可以供給12歲-17歲,且體重至少40公斤的孩子使用。
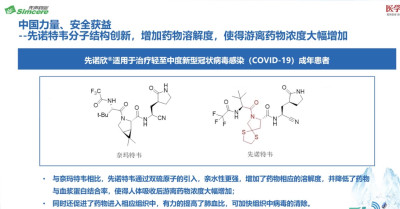
$先聲藥業(HK|02096)$ 先諾欣(先諾特韋片/利托那韋片組合包裝)的先諾特韋與的$輝瑞(NYSE|PFE)$ 的paxlovid(奈瑪特韋/利托那韋)的奈瑪特韋相比,先諾特韋通過雙硫原子的引入,親水性更強,增加了藥物相應的溶解度,並降低了藥物與血漿蛋白結合率,使得人體吸收後遊離藥物濃度大幅增加;同時還促進了藥物進入相應組織中,有力的提高了肺血比,可加快組織中病毒的清除。
追加內容
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:5月25日,美國食品和藥品管理局(FDA)正式批准輝瑞(NYSE:PFE)的新冠
地址:https://www.breakthing.com/post/63734.html







