


中國基金報記者 米洛
取道港股後,百奧賽圖依然把科創板作爲最終目的地。
6月20日,上交所披露的發行上市審核信息顯示,百奧賽圖的科創板上市申請已經獲得受理。
此時,距離百奧賽圖登陸港交所,僅僅過去了8個多月。
早在2021年2月,百奧賽圖曾和中金公司籤訂上市輔導協議,擬赴科創板上市。同年8月,公司終止了輔導工作,轉而在2022年9月投奔港股市場。
可在登陸港股市場後,百奧賽圖依然對科創板“無限眷戀”。3月6日,公司宣布擬發行A股並在科創板上市。時間過去3個月,公司的科創板上市申請已經獲得受理。
在此次招股書中,百奧賽圖明確提出,公司基於自主开發的基因編輯技術提供各類創新模式動物以及臨牀前階段的醫藥研發服務。
這意味着,一旦公司登陸科創板,A股將迎來“基因編輯第一股”。
科創板大筆募資爲建房?
作爲擬快速兩地上市的生物醫藥公司,百奧賽圖在港股和科創板的募資投向有着明顯的差別。
此次赴科創板IPO,百奧賽圖擬募資18.93億元,用於藥物早期研發服務平台建設項目、抗體藥物研發及評價項目、臨牀前及臨牀研發項目和補充流動資金。
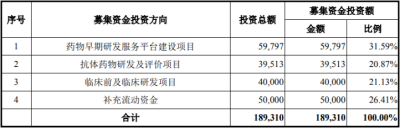
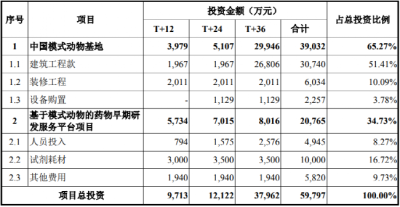
具體來看,藥物早期研發服務平台建設項目投資爲5.98億元,其中大部分爲建築工程款、裝修款。
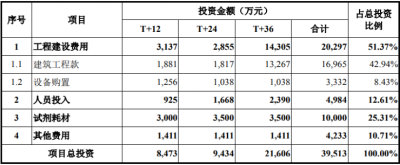
抗體藥物研發及評價項目總投資爲3.95億元,工程建設款依然是主要部分。
臨牀前及臨牀研發項目總投資爲4億元,推進公司目前處於臨牀前研究及臨牀試驗階段的候選藥物研究,同時在未來發現並挑選出有效性和安全性表現最佳的候選分子作爲候選藥物進行开發。
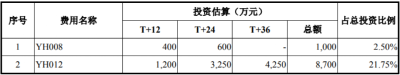
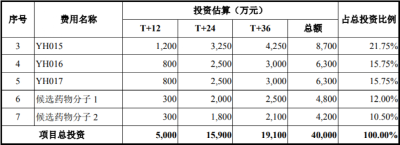
將這些募投項目與不久前,公司在港股上市時的募投項目做對比,不難發現其中的差別。
去年在港股IPO時,百奧賽圖募集資金爲5.41億元,其中大部分用於核心產品進一步研發(YH003、YH001),少部分用於“千鼠萬抗”計劃。

由此可見,百奧賽圖在科創板募資金額明顯高於在港股募資金額,而且多出來的部分,大部分用於工程建設、裝修等方面,直接投向研發的並不多。
招股書顯示,其擬通過在科創板募集的資金,將建設約11萬平方米的建築及室外配套工程,其中7.5萬平方米位於海門市,3.5萬平方米位於北京大興。
百奧賽圖爲外界所熟知,是其提出的“千鼠萬抗”計劃,即對 1000 余個潛在抗體藥物靶點的抗體藥物進行規模化的篩選、驗證與开發。
在此次招股書中,百奧賽圖表示,公司是一家臨牀前 CRO 以及生物醫藥企業,公司基於自主开發的基因編輯技術提供各類創新模式動物以及臨牀前階段的醫藥研發服務,並利用其自主开發的 RenMice 全人抗體小鼠平台針對人體內千余個潛在藥物靶點進行規模化藥物發現與开發,並將有潛力的抗體分子進行對外轉讓、授權或合作开發。
目前,公司的業務主要分爲基因編輯服務、臨牀前藥理藥效評估服務、模式動物銷售、抗體开發及創新藥开發。
由於仍處於前期研發投入中,百奧賽圖的財務數據並不好看。
2020年至2022年,公司淨利潤分別爲-47669.20 萬元、-54564.26 萬元、-60215.69 萬元,而研發投入佔據了成本的大頭。2020年至2022年,公司研發投入分別爲 27630.62 萬元、55848.48 萬元、69916.74 萬元。
雖然連年大額虧損,但資本市場仍對其後續業務存在期待。在港股市場,百奧賽圖的發行價格爲25.22港元/股。只是,時至今日,公司股票最新收盤價爲21.45港元/股,仍處於破發的狀態。根據最新收盤價,百奧賽圖的總市值爲86億港元。
由於研發投入巨大,而謀求多地上市,已經成爲生物醫藥公司的普遍共識,百濟神州、君實生物等公司已經這么做了。
只是,研發投入最終能帶來多少回報?
業內人士表示,靶點的挑選至關重要,不僅關系研發難度,更決定了研發成功後的市場規模。
目前,百奧賽圖已有 10 個管线產品,其中 5 個處於臨牀試驗/IND 獲批階段。公司已針對 YH001、YH002、YH003、YH008 以及 YH011分別與 Tracon Pharmaceuticals、Syncromune Inc.、ISU Abxis、微芯新域以及啓德醫藥進行合作研發,並將 YH005 產品开發及商業化權益授權給榮昌生物。

其中,YH003 爲發行人研發的新型靶向 CD40 的重組人源化激動性 IgG2 單抗,主要开發用於胰腺導管腺癌、黏膜型黑色素瘤等適應症。目前,全球尚無獲批的 CD40 抗體藥物,因此,競爭格局較好。
只是,這一市場規模不大。據預測,中國 CD40 腫瘤抗體藥物的市場規模將於 2026 年增至 6 億人民幣,2030 年將進一步增加到 47 億人民幣。
與之相比,YH001(人源化抗 CTLA-4 IgG1 單克隆抗體)面對的市場空間更大。2022 年,全球 CTLA-4 腫瘤抗體藥物市場爲 21 億美元。預計 2026 年將增至 52 億美元,2022-2026 年的復合年增長率爲 25%。預計 2026 年,中國 CTLA-4 腫瘤抗體藥物市場將增長至 60 億人民幣。
只是,全球共計兩種 CTLA-4 單抗獲得美國 FDA 批准上市,分別爲伊匹木單抗(商品
名:Yervoy)及替西木單抗(商品名:Imjudo)。2021 年,伊匹木單抗獲中國 NMPA 批准上市,用於治療胸膜間皮瘤,爲目前國內唯一獲批的 CTLA-4 單抗。
編輯:艦長
審核:許聞
版權聲明
《中國基金報》對本平台所刊載的原創內容享有著作權,未經授權禁止轉載,否則將追究法律責任。
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:“基因編輯第一股”,要火速回A!募資額是前次3.5倍,爲增11萬平辦公面積?
地址:https://www.breakthing.com/post/71211.html







