
CD47靶點被稱爲“下一個PD-1”,可研發之路卻一波三折、“難倒英雄漢”。
從再鼎到羅氏,再從艾伯維到吉利德,不是對CD47抗體降級开發,就是放棄开發,甚至因療效不足終止开發。
新藥开發的目的在於爲患者提供安全、有效的治療方案。爲了達到這兩項指標,CD47抗體研發已經走過了一段又一段坎坷的路途。
一、CD47靶點:泛癌藥潛力,國內布局藥企超30家
與PD-1一樣,CD47靶點也能廣泛表達在不同的癌細胞,因此成爲了後PD-1時代的明星靶點。
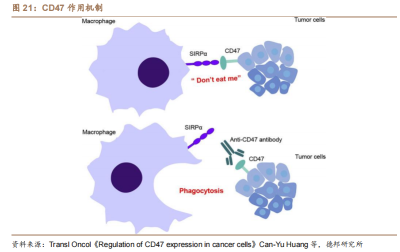
從作用機制看,CD47可以和巨噬細胞表達的SIRP相結合,釋放“別喫我”信號,進而阻斷巨噬細胞對腫瘤細胞的吞噬作用。研究者認爲抑制癌細胞中CD47信號可能促進巨噬細胞對腫瘤細胞的吞噬,從而限制腫瘤生長。
簡而言之,CD47可以阻止巨噬細胞吞噬和破壞腫瘤細胞。
此外,CD47成爲新一代免疫療法熱門靶點的另一個重要原因,更在於PD-1的內卷、急需新的前沿靶點替代,以及自身釋放出的極大的市場潛力。
正是看中CD47被开發爲泛癌藥的潛力,財大氣粗的國外頭部玩家掀起了資本熱潮。
例如,吉利德於2020年3月斥資49億美元收購了Forty Seven,將明星藥物IgG4 CD47單抗Hu5F9-G4(Magrolimab)納入囊中;同年9月,艾伯維與天境生物達成交易總額近30億美元的license-in交易;輝瑞於2021年8月斥資近23億美元對價收購了Trillium,並囊獲靶向CD47腫瘤免疫在研療法。
這些巨額交易,不僅將CD47抗體研發推向了最高潮,還吸引了無數後來者前僕後繼地湧入這條賽道。
除了上述三家國外頭部玩家以外,目前國內CD47抗體藥物賽道已遍地开花。據Insight數據庫顯示,當前已有36款產品進入臨牀階段,涵蓋單抗、雙抗和融合蛋白等藥物類型,布局企業涉及天境生物、康方、信達、天廣實、百奧泰等超30家企業。

國內進入臨牀階段CD47單特異性抗體 來自:Insight 數據庫網頁版(下文如無特殊標注,爲同一來源)
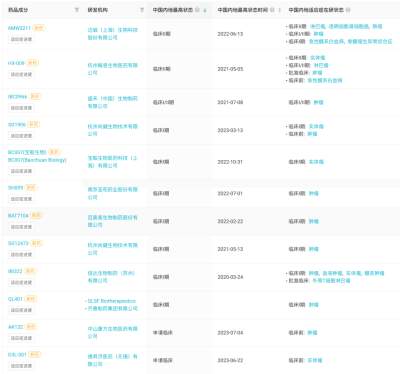
國內進入臨牀階段CD47雙特異性抗體
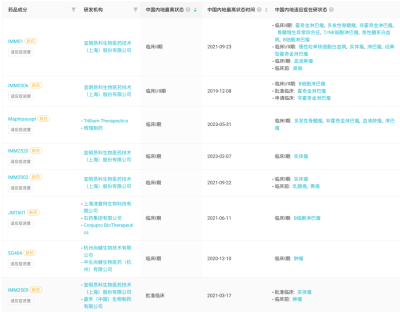
國內進入臨牀階段CD47抗體類融合蛋白
實際上,理想很豐滿,現實卻很骨感。CD47抗體研發,並沒有想象中的那般順利。
二、CD47抗體研發的“攔路虎”:安全性、療效
布局者衆,成功者少,是當下CD47抗體研發的殘酷現狀。
CD47抗體研發的第一道難關,就在於安全性。
由於CD47在人體內紅細胞上廣泛表達,靶向CD47藥物在殺傷腫瘤時會導致紅細胞的吞噬破壞和凝集,誤傷紅細胞,影響其使用的安全性和耐受性,造成貧血、血小板減少症等血液毒性問題。
例如,Arch Oncdogy的Ti-061、新基公司(Celgene)的CC-90002和Surface Oncology的SFR231,都因發生嚴重溶血反應導致臨牀失敗。
如何在保護紅細胞的同時,最大程度地殺傷腫瘤細胞,成爲CD47抗體研發的核心關鍵。
爲了降低藥物紅細胞毒性並提高療效,吉利德Magrolimab在Fc端採用了IgG4亞型而非IgG1亞型,由於IgG4亞型不能引發強烈的ADCC和CDC效應,降低了對紅細胞、血小板的影響,並且通過預激給藥的方式來解決血液毒性的問題。
實際上,這種解決方案的確獲得了良好的安全性數據:根據Forty Seven公司在2019年ASH會議上公布的Magrolimab和阿扎胞苷聯合治療高風險AML(急性髓系白血病)和MDS(骨髓增生異常綜合徵,無法進行誘導化療的患者)臨牀Ib期研究結果顯示,在62例患者中只有1例(1.6%)因治療相關不良事件停止治療。
當時正是基於這項優異的數據,吉利德才斥資49億美元收購Forty Seven。
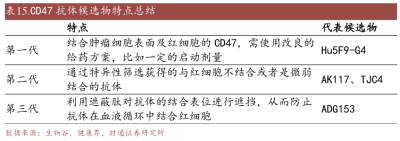
之後,吉利德在萬衆矚目中开啓了Magrolimab聯合阿扎胞苷聯合治療MDS的Ⅲ期臨牀試驗。這也是驗證CD47靶點成藥性最接近成功的一次。
事實上,新藥研發總是充滿坎坷。
7月21日,吉利德在萬衆期待下遺憾宣布:因在中期分析中發現聯合療法有效性不足,終止Magrolimab聯合阿扎胞苷聯合治療MDS的Ⅲ期臨牀試驗。
好不容易邁過了安全性這道坎,卻因療效不足栽了。這便是CD47抗體研發要跨越的第二道難關:療效。
雖然Magrolimab在Fc端採用IgG4亞型,確實提高了安全性。但與此同時,由於IgG4 Fc只傳遞適中的信號,導致CD47單抗對腫瘤細胞的殺傷能力被大幅度削弱。
單藥使用效果有限,藥效也降低。這也是爲何研發靶向CD47藥物要採取聯合用藥,或开發基於CD47的雙抗的緣故。
三、“全村的希望”:天境、康方、$信達生物(HK|01801)$能否逆襲?
窮且益堅,不墜青雲之志。
盡管Magrolimab已經在MDS適應症上宣告失敗,但吉利德還在开發10多項涵蓋血液瘤和實體瘤適應症,其中就包括“硬骨頭”AML(急性髓細胞性白血病)。
AML是成人中最常見的急性白血病類型,約佔成人白血病的70%。據統計,我國AML的發病率約爲2.57/10萬人,死亡率約爲每年1.57/10萬人。現有治療方案阿糖胞苷化療和造血幹細胞移植治療,雖然有效延長了患者生存期,但數據都不算驚豔。就看吉利德能否再次創造奇跡了。
雖然羅氏、艾伯維和吉利德等國外頭部玩家接連受挫,但CD47抗體研發進展靠前的天境生物、信達生物和康方生物,還有機會成爲“全村的希望”。
例如,$天境生物(NASDAQ|IMAB)$的來佐利單抗(lemzoparlimab)雖然也採用了IgG4亞型抗體,但卻利用其獨有的人源天然噬菌體技術,篩選出了可以結合在稀有表位上的CD47抗體,通過降低與紅細胞的結合解決血液毒性的問題。
不過,正如前文所述,這種採取IgG4亞型抗體的解決方案,存在藥效降低的缺陷。就看天境生物如何解決這一問題。
值得一提的是,Lemzoparlimab並沒有放棄MDS適應症。而且,根據天境生物近期投資者文檔,該藥與Magrolimab療效相當的同時安全性可能更優,與紅細胞結合更低。

來自:天境生物官網資料
另外,Trillium(被輝瑞收購)的產品TTI-621,也採取了這種降低CD47對紅細胞的結合能力的解決方案。
$康方生物(HK|09926)$的AK117(萊法利單抗)也有着獨特的結構設計,屬於新一代人源化IgG4 mAb,無血凝作用,可誘導巨噬細胞對腫瘤細胞的強大吞噬作用,無需較低的預劑量來預防貧血,且抗腫瘤活性良好。
不僅如此,無論單藥或聯合化療、聯合雙抗化療,AK117在血液瘤或實體瘤中總體安全性良好且無種族差異,並且不需要預激給藥。
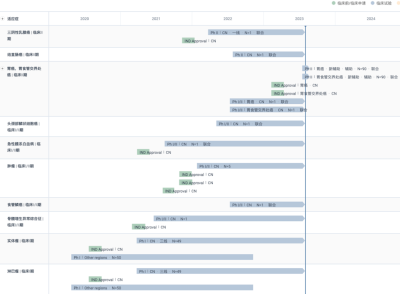
AK117全球項目开發進度甘特圖
值得一提的是,目前針對三陰乳腺癌治療的CD47靶向藥物只有AK117,而且聯合阿扎胞苷治療MDS、AML適應症的研究均已進展到臨牀Ib/II期階段。

AK117針對 MDS、AML臨牀試驗
綜上可見,獨特的結構設計,確實呈現出一定的差異化優勢。但最終能否成藥,仍需時間來檢驗。
四、尾聲
總結來看,CD47抗體研發確實面臨諸多坎坷,即便是羅氏、艾伯維、吉利德等頭部玩家也接連受挫。當然,即便是過去如日中天的PD-1,研發之路也曾布滿荊棘和坎坷。
從現有的解決方案看,獨特的結構設計、聯合用藥或玩法更高級的雙抗,期待能走出不一樣的風景。
參考資料:
1、《康方生物-B-9926.HK-自主商業化驗證+大單品出海,持續進化的新一代創新藥龍頭》,德邦證券
2、《屢敗屢战,CD47靶點是否還有未來?》,同寫意,2023-01-28
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:CD47賽道風雲:攻克“下一代PD-1”,天境、康方打響逆襲战
地址:https://www.breakthing.com/post/83951.html







