
據衆成醫械統計:2022年4月第2周,共8條醫械企業動態資訊!
4月第2周醫械企業動態盤點
1、开立醫療HD-550電子內窺鏡系統獲美國FDA批准

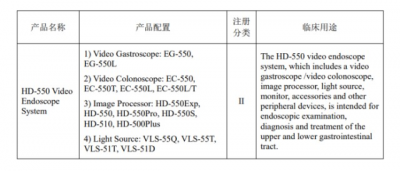
开立醫療公告稱,其HD-550電子內窺鏡系統已於4月1日獲美國FDA批准,於近日取得FDA 510(k) SE Letter。(來源:深圳證券交易所)
看點
公告顯示,HD-550系列是开立醫療在2018年推出的全高清電子內鏡系統,產品技術處於國際先進、國內領先水平。美國內窺鏡市場是全球最重要的消化內鏡市場之一,HD-550系列獲得FDA批准,將有利於开立醫療內窺鏡產品在北美市場乃至國際市場發揮影響力,獲得更多全球市場份額。
2、“微創系”分拆上市又一例,微創電生理科創板IPO“提交注冊”

4月2日,上海微創電生理醫療科技股份有限公司(下稱“微創電生理”)科創板IPO“提交注冊”。3月31日,微創電生理科創板首發獲通過。截至目前,電生理醫療科技已完成三輪問詢回復。(來源:資本邦)
看點
根據招股書,微創電生理主營心髒手術方案,如快速性心律失常,是國內首個能提供三維技術、設備、耗材的國產廠商。2020年,其三維系統產品已獲批上市,該產品也是第一個國產的磁電雙定位系統。此外,微創電生理也是第一家通過”標准五“上市的未盈利醫療器械企業。
3、天益醫療將於4月7日在深交所創業板上市

天益醫療發布公告稱,經深圳證券交易所審核同意,公司發行的人民幣普通股票將於2022年4月7日在深圳證券交易所創業板上市。(來源:深圳證券交易所)
看點
天益醫療是一家三類醫用耗材生產企業。該公司集研發、生產、銷售於一體,致力於醫療器械的生產。主要產品有體外循環血液處理設備、喂食器械及導管、物理治療及康復設備、醫用高分子材料及制品、病房護理設備及器具等。
4、歐普康視“硬性接觸鏡衝洗液”首次注冊完成

4月6日,歐普康視發布公告稱,於近日收到安徽省藥品監督管理局換發的《醫療器械生產許可證》,完成了醫療器械生產產品更新登記。此次生產許可證變更系因公司申請的第三類醫療器械產品“硬性接觸鏡衝洗液”首次注冊完成而進行的相應變更。(來源:深圳證券交易所)
看點
據悉,該產品爲境內首款三類醫療器械硬鏡衝洗液,目前境內尚無其他硬鏡衝洗專用的三類醫療器械產品。
5、揚州洋生醫藥科技有限公司召回一次性使用連接管
日前,揚州洋生醫藥科技有限公司報告,該企業接到醫療機構不良事件報告,一次性使用連接管的三通閥在使用過程中可能出現連接不緊密的情況,個別產品有漏液問題,現主動召回,召回級別爲三級。(來源:國家藥品監督管理局)
看點
此次召回涉及3個批次15000只一次性使用連接管。
6、熱景生物一新冠抗原檢測產品獲得香港政府衛生署認證

4月7日傍晚,熱景生物發布公告稱,公司於近日獲得香港政府衛生署醫療儀器科批准新冠抗原檢測試劑一項,該試劑盒用於通過前鼻腔拭子,體外檢測人體內新型冠狀病毒抗原,適用於新型冠狀病毒疑似病例快速篩查,用於居家自由檢測。(來源:上海證券交易所)
看點
該產品獲得香港政府衛生署醫療儀器科認證批准後,可在香港特別行政區和認可香港政府衛生署醫療儀器科認證的國家及地區進行銷售。
7、微波消融器械开發商百德醫療二次遞表港交所

據港交所4月7日披露,百德醫療投資控股有限公司向港交所主板提交上市申請,中銀國際與中泰國際爲聯席保薦人。該公司曾於2021年9月28日向港交所遞表,而後失效。(來源:智通財經網)
看點
百德醫療是腫瘤微創治療的微波消融醫療器械的开發商及提供商,其產品供應及管线產品主要包括微波消融治療儀以及與治療儀配合使用的微波消融針。
8、之江生物獲得國家三類醫療器械注冊證及五項歐盟CE認證

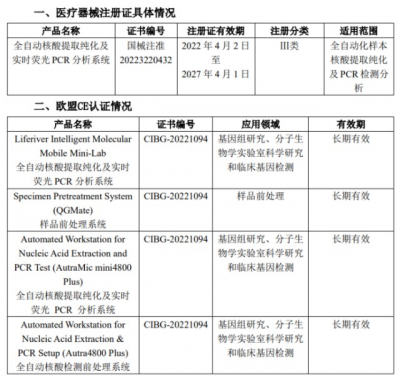
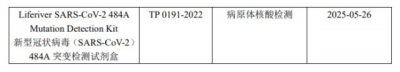
4月8日,之江生物發布公告稱,公司及全資子公司上海之江生物醫藥科技有限公司於近期獲得六項相關認證或注冊,其中一項爲國家三類醫療器械注冊證,其余五項爲歐盟CE認證。(來源:上海證券交易所)
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:开立醫療HD-550電子內窺鏡系統獲美國FDA批准|4月第2周企業動態盤點
地址:https://www.breakthing.com/post/8557.html







