
1月27日,在名爲B. Riley Securities的2022年虛擬腫瘤投資者大會上,TG公司CEO Michael Weiss表示,美國FDA部分暫停了U2組合Ukoniq(umbralisib)聯合ublituximab治療慢性淋巴細胞白血病(CLL)和非霍奇金淋巴瘤(NHL)的研究。受此消息影響,該公司股價大跌40%。
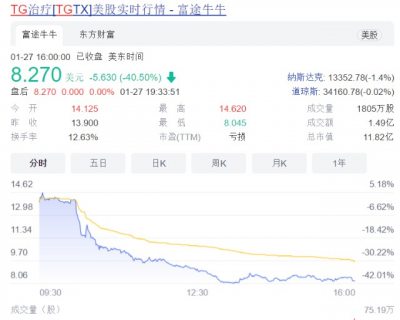
“部分治療CLL和NHL的試驗將不再招募新患者,但已獲益的患者可繼續試驗。”他補充說,該決定不是基於新的信息,而是源於先前的擔憂,即關於UNITY-CLL試驗總生存率的早期分析。這一擔憂將在3月或4月召开的腫瘤藥物咨詢委員會會議上討論。
早在2021年9月,TG公司收到FDA的回信,FDA表示將召开專家咨詢委員會討論U2組合治療CLL和SLL的BLA申請。原因是,截至FDA審查期間要求的總體生存分析截止日期2021年9月,U2組合在總生存期方面與活性對照組相比未顯示出顯著性差異。目前,在該公司表示正准備向FDA提交UNITY-CLL試驗更新的總生存期分析數據。
Umbralisib已於2021年2月獲批用於復發/難治性(R/R)邊緣區淋巴瘤(MZL)和濾泡性淋巴瘤(FL),是FDA批准的首款PI3K/CK1抑制劑。Ublituximab是一款在研新型CD20單抗,二者的組合被稱爲U2。
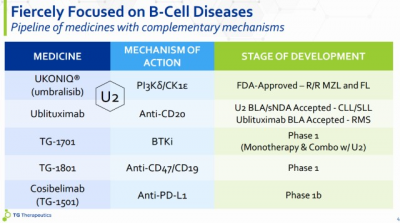
基於III期UNITY-CLL試驗結果,2021年5月,FDA受理了U2組合治療CLL和SLL的BLA申請,PDUFA日期爲今年3月25日。結果顯示,U2組合相較於苯丁酸氮芥+奧妥珠單抗顯著改善患者PFS,mPFS分別爲31.9月和17.9月。

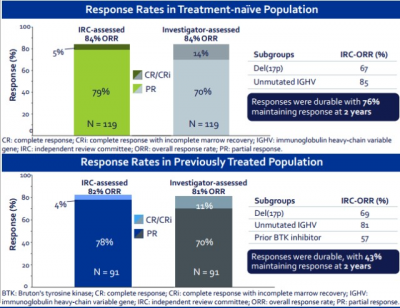
2021年ASH會議上,UNITY-CLL試驗數據更新,U2在TN(此前未接受過治療)人群中的無進展生存期(PFS)爲38.5個月,2年PFS爲76.6%,ORR爲84%,CR/CRi爲5%。在PT(經治)人群PFS爲19.5個月,2年PFS爲41.3%,ORR爲82%,CR/CRi爲4%。
U2聯合療法治療血液腫瘤是TG公司重要布局,目前還在开展聯合TG-1701 (BTKi)以及維奈克拉(Bcl-2i)的臨牀研究。


溫馨提示
醫藥魔方Info關注全球範圍內的重要醫藥信息情報,包括藥品注冊審批、藥物臨牀試驗數據、公司交易並購動態、公司財報業績、醫藥人才流動,熱門政策事件等等,爲用戶的日常決策提供關鍵信息參考。讓你充電5分鐘,吹牛2小時!
星標醫藥魔方Info,這樣就不會錯過我們的推送啦~
操作步驟見上圖:1)點擊標題下方“醫藥魔方Info”,2)至右上角“…”,3)設爲星標

醫藥魔方Info
傳遞醫藥信息,分享資源數據!醫藥魔方Info關注全球範圍內的重要醫藥信息情報,包括藥品注冊審批、藥物臨牀試驗數據、公司交易並購動態、公司財報業績、醫藥人才流動,熱門政策事件等等,爲用戶的日常決策提供關鍵信息參考。讓你充電5分鐘,吹牛2小時!
1331篇原創內容
Official Account
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:TG公司U2組合臨牀試驗遭FDA部分暫停,股價大跌40%
地址:https://www.breakthing.com/post/1620.html







