
繼被歐盟監管部門提示存在甲狀腺癌風險後,丹麥藥企諾和諾德(Novo Nordisk)旗下兩款GLP-1類藥物又因可能存在的輕生風險而遭歐盟調查。GLP-1藥物的吸金能力已無需證明,在正大天晴、恆瑞、信達生物、禮來等衆多本土、跨國藥企競相入局GLP-1藥物市場的同時,也有輝瑞、阿斯利康等知名藥企先後停止开發其部分GLP-1藥物,翰宇藥業主動撤回利拉魯肽注射液的上市注冊申請……GLP-1類藥物未來市場如何?
諾和諾德兩款GLP-1明星藥再遭質疑
據路透社7月10日報道,歐盟藥品監管局(EMA)正在調查諾和諾德旗下兩款藥物,包括糖尿病藥物Ozempic(司美格魯肽)和減肥藥物Saxenda(利拉魯肽)。調查的原因是冰島監管部門報告了三例患者使用這些藥物後出現輕生念頭的案例,其中包括兩個使用Ozempic的患者案例以及一個使用Saxenda的患者案例。
這並非諾和諾德的藥物首次被歐盟質疑。6月22日,據fiercepharma報道,歐洲藥品管理局(EMA)已將GLP-1藥物標記爲甲狀腺癌的潛在風險,包括諾和諾德的Ozempic和Wegovy,以及禮來的Mounjaro。監管機構要求公司在7月26日之前提交更多信息。
對於甲狀腺風險,諾和諾德方面回應稱,試驗和上市後監測的安全數據並未發現該藥物與甲狀腺癌之間存在因果聯系。對於此次自殺風險相關的問題,諾和諾德在10日的一份聲明中同樣強調,至今爲止,其自身的安全監測並未發現患者的自殺念頭與藥物之間存在“因果關系”。不過,諾和諾德也強調,患者安全是重中之重,並且非常嚴肅地對待所有有關不良事件的報告。
下一個降糖王者,有人入場,有人撤退
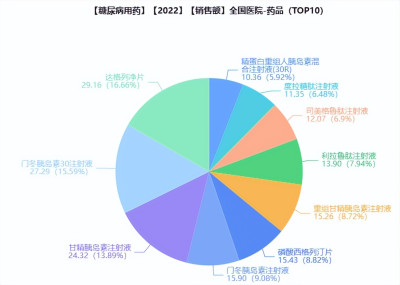
據藥融雲全國醫院銷售數據庫,2022年糖尿病用藥市場份額最高的藥品TOP10中,胰島素及其同系物佔據5席。但隨着門冬胰島素、甘精胰島素、賴脯胰島素專利陸續過期,胰島素市場勢必走向萎縮,GLP-1和SGLT2等新一代降糖產品日漸成爲降糖藥市場的“必爭之地”。
2022年,全球糖尿病藥物的市場規模爲596億美元,其中銷售額前2位爲司美格魯肽和度拉糖肽,均爲GLP-1受體激動劑。其中司美格魯肽專利將於2026年到期,也給了國產司美格魯肽機會。目前九源基因、中美華東、麗珠集團均在跟進研發,並已進入臨牀階段。
總體來看,GLP-1受體激動劑是目前全球市場佔有率最高的非胰島素類糖尿病藥物。目前國內已有8款GLP-1藥物獲批上市,均已進入醫保。其中四款爲短效注射劑,包括需要每日1~3次皮下注射的短效注射劑,艾塞那肽、利拉魯肽、貝那魯肽和利司那肽;另外四款爲長效注射劑,分別是艾塞那肽微球、度拉糖肽、洛塞那肽和司美格魯肽(索馬魯肽)。
值得一提的是,近日華東醫藥發布公告稱,全資子公司杭州中美華東制藥有限公司申報的利拉魯肽注射液肥胖或超重適應症的上市許可申請獲得批准。而在今年3月底,華東醫藥的利拉魯肽注射液才剛剛獲批用於治療糖尿病。
此次獲批意味着,除原研企業外,中美華東將成爲中國大陸唯一一家擁有利拉魯肽注射液糖尿病適應症上市批文的企業,也是中國大陸首家擁有利拉魯肽注射液肥胖或超重適應症上市批文的醫藥企業。
有人激流勇進,也有人止步轉身。
7月1日,翰宇藥業公告,已主動撤回利拉魯肽注射液的上市注冊申請。國際制藥巨頭輝瑞此前也重金投入GLP-1類藥物研發,但在6月27日,輝瑞卻發布公告稱,停止开發其尚處於臨牀試驗階段的肥胖症和糖尿病藥物Lotiglipron,理由是,在中期臨牀研究中,服用該藥的患者轉氨酶升高,這是肝細胞受損的信號。
在發布信息當天,輝瑞公司股價盤中一度跌到5.59%。在輝瑞發布這一公告之前,阿斯利康也曾發布公告放棄其一款處於开發中後期GLP-1R/GCGR激動劑,以及一款口服GLP-1R激動劑AZD0186。
超百款GLP-1新藥,恆瑞、信達……火熱研發中
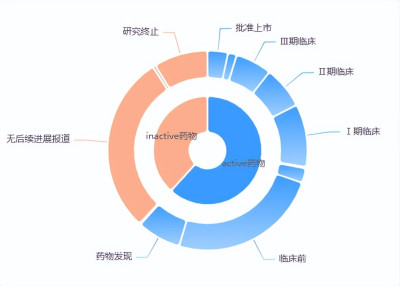
盡管如此,GLP-1藥物的研發依舊火熱,據藥融雲數據庫統計,目前已有超百款藥物進入臨牀及以上階段。其中禮來的GLP-1R/GIPR雙靶點激動劑替爾泊肽(Tirzepatide)已在華遞交上市申請,有望今年獲批。國內恆瑞、正大天晴、信達生物等多家藥企早早布局靶向GLP-1受體激動劑、尤其是GLP-1多靶點藥物,競爭格局逐漸白熱化。以下這些藥企/品種尤其引人關注。
全球GLP-1藥物研發狀態
信達生物:IBI362
這是信達生物與禮來制藥共同推進的一款與哺乳動物OXM類似的長效合成肽(OXM3),在同類產品中具有最優潛力。同時,IBI362有望成爲國產第一款雙靶點降糖減肥新藥。
2023年1月,信達生物宣布GLP-1/GCGR雙激動劑IBI362在兩項Ⅲ期臨牀中完成首例受試者給藥。其中DREAMS-1將進一步驗證在單純飲食運動控制不佳的中國2型糖尿病患者中,mazdutide長期給藥的療效及安全性;DREAMS-2將進一步驗證mazdutide的療效及安全性,並比較mazdutide與度拉糖肽的療效及安全性。
銀諾醫藥:蘇帕魯肽
2023年1月,銀諾醫藥宣布了蘇帕魯肽的兩項III期臨牀試驗達到主要療效終點,這兩項臨牀研究將於2023年2季度完成,並於2023年3季度獲得主要臨牀結果。蘇帕魯肽有望成爲國內首個自主知識產權的人源、長效GLP-1受體激動劑。
華東醫藥:SCO-094
2021年6月,華東醫藥以400萬美元的首付款,從日本SCOHIA pharma公司引進了GLP-1/GIP受體雙靶點激動劑SCO-094。同年的4月,華東醫藥還收購了擁有2款GLP-1R/GIPR激動劑的道爾生物。今年2月,中美華東和SCOHIA籤署了新的合作協議,將合作範圍進一步擴大,中美華東將獲得SCO-094及其衍生產品在全球(包括日本)的獨家开發、生產及商業化權益。
鴻運華寧:格魯塔珠單抗
據藥融雲數據庫,鴻運華寧的重組抗人GLP-1受體人源化單克隆抗體注射液(格魯塔珠單抗,GMA102)針對2型糖尿病的研究最高已至III期臨牀階段;針對超重或肥胖的研究已進行至II期臨牀階段。

翰森制藥:HS-20094
這是一款GIP/GLP-1R雙靶點藥物,爲每周1次的皮下注射制劑,已於今年5月啓動II期臨牀試驗,旨在2型糖尿病受試者中評價HS-20094多次給藥的安全性、耐受性、藥代動力學和藥效學。
東陽光藥:HEC88473
東陽光藥的HEC88473是國內首個獲批臨牀的GLP-1/FGF21雙重激動劑,目前處於I期臨牀研究階段。據悉,FGF21是一種可以調節糖脂代謝的內分泌激素,臨牀有多款FGF21單靶點藥物在NASH、2型糖尿病、肥胖以及肝纖維化等適應症中取得了初步的研究進展。
<END>
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:明星藥再遭質疑?諾和諾德旗下兩款GLP-1藥物被歐盟調查!
地址:https://www.breakthing.com/post/77177.html







