

作者|《未來跡》陳龍
“在嬰童產品中疑似添加他克莫司,行爲十分惡劣,令人感到意外、震驚和憤慨。”近日,一款名爲“紅色蝸牛嬰初霜”的嬰童類產品被曝疑似違法添加抗生素成分,在化妝品業內引起軒然大波。
就在昨日(7月13日),此事件有了新進展。
浙江臨海市市場監督管理局在當地官方媒體平台《臨海24小時》發布消息稱:接廣東省藥品監督管理局信息,根據輿情和初步調查情況,標示"產品名稱:紅色蝸牛嬰初霜"、標示"備案人/生產企業:廣州中浩生物科技有限公司"(以下簡稱中浩生物)的化妝品,備案編號爲“粵 G 妝網備字2022312819”,涉嫌非法添加“他克莫司”。

據悉,臨海3家經營單位庫存共計有上述紅色蝸牛嬰初霜10盒,分屬3個不同批次,執法人員對上述產品進行現場抽樣並送至檢測機構進行檢驗,由臨海局三批送檢產品均檢出“他克莫司”,相關案件线索正在國家局的統一協調指揮下全國聯動核查處置中。
與此同時,國家藥品監督管理局官網顯示,上述紅色蝸牛嬰初霜產品備案已於7月13日被注銷,與此同時,涉事企業中浩生物旗下多款嬰童護理產品備案也在同日注銷,涉及“杏修璞護霜”、“嘟卡珍膚霜”、“菲諾熊草本嬰膚霜”等多款相對熱門的產品。
網紅嬰童霜中疑似添加違禁藥物成分
隨着臨海市市場監督管理局的消息發布,紅色蝸牛嬰初霜是否添加他克莫司的真相已近在咫尺。據消息分析,多地職能機構已經在統一部署下對該產品進行核查,並要求門店停售相關產品。
《FBeauty未來跡》對此事的發展進程詳細梳理如下:
7 月4日,知名測評博主“老爸測評”曝出知名的兒童面霜產品紅色蝸牛嬰初霜違規添加抗生素他克莫司。經由消費者舉報之後,“老爸測評”團隊在紅色蝸牛官方旗艦店購买樣品後,委托第三方實驗室檢測。檢測結果顯示該兒童面霜產品添加了0.034%的他克莫司成分。
隨後,紅色蝸牛官方旗艦店已將所有產品下架,但依舊有少量线上店鋪仍在銷售該款嬰初霜產品。
對此,該產品品牌方中浩生物對外發布聲明予以回應。

該聲明核心內容如下:
1.宣稱“檢測報告不實”,“老#測評”抖音號捏造事實,送檢產品來源不明。
2.紅色蝸牛嬰初霜經是經過藥監局備案的產品,每個批次都經過嚴格檢測,檢測100多種激素成分,均未發現任何違規添加劑。
3.他克莫司爲防止器官移植排異反應的藥物,並非治療皮膚問題成分。
4.公司已將近一年所有批次產品送由國家權威機構檢驗,並將公布檢驗結果,以正視聽。
整篇聲明中並未對紅色蝸牛產品中是否添加他克莫司成分給出正面回應。
7月7日,國家藥監局發布《化妝品中他克莫司和吡美莫司的測定》化妝品補充檢驗方法的公告,對於膏霜乳類、液體(水、油)類化妝品中他克莫司和吡美莫司的定性和定量測定給予官方的標准。
據2021年發布的《化妝品補充檢驗方法管理工作規程》顯示,化妝品補充檢驗方法可用於化妝品的抽樣檢驗、質量安全案件調查處理和不良反應調查處置,其檢驗結果可以作爲執法依據。《化妝品安全技術規範》(2015年版)中就明確規定:抗生素類物質禁止被添加到化妝品中。
結合兩條法規可以認定,在化妝品中添加大環內酯類抗生素“他克莫司”系違法行爲,同時檢驗機構也可依據公告對他克莫司進行專項檢測。
7月10日,廣州市市場監督局工作人員就此事回復揚子晚報,該局相關部門已對此事件立案調查。
7月13日,臨海市市場監督管理局在《臨海24小時》發布消息稱,當地於7月6日根據國家、省、市局的統一部署追溯相關產品並將產品送檢,檢驗結果顯示產品中添加他克莫司。
7月13日,涉事企業廣州中浩生物科技有限公司旗下包括紅色蝸牛兒童嬰初霜在內的多款產品備案被注銷。
截至目前,中浩生物旗下多款備案被注銷的產品已經被商戶下架。有經銷商表示,自己並未得到產品備案注銷消息,且目前無法聯系到中浩生物廠商,相關負責人電話一直處於忙线中。
違法添加“他克莫司”的危害超出想象
國家藥品監督管理局的公告和相關職能機構執法動作來得如此迅速且極具針對性,足見監管機構對此事的重視程度,而此次疑似違規添加的他克莫司也確實值得這樣的重視。
公开資料顯示,他克莫司(Tacrolimus FK506)是一種從鏈黴菌發酵物中提取的大環內酯類抗生素,主要通過抑制白介素-2的釋放全面抑制T淋巴細胞的作用,具有強大的免疫抑制作用,其免疫抑制作用約是環孢素(CsA)的10-100倍[1]。
這款抗生素被主要應用於器官移植手術後的抗排異反應,也被當作處方藥,用於激素類藥物無法治療的皮膚疾病,主要通過抑制免疫反應的方式來達到治療效果,對用量和使用方法都有嚴格要求,即便作爲外用藥品,也不可用於2歲以下兒童的皮膚疾病。
雖然在嬰童護理產品中添加抗生素系違規行爲已經是不爭的事實,但在兒童護膚品中違法添加他克莫司的潛在風險卻仍然有些“超乎想象”。
無論是放眼歐美國家的監管,還是我國皮膚科醫師、護膚專家等專業研究來看,當此成分被添加進嬰童護理產品中後,可能會導致比激素成分更嚴重的後果,比如致癌風險。
早在2005年3月,美國 FDA 就曾向醫生發出警告由於他克莫司(商品名 Protopic)存在潛在致癌危險。FDA要求必須在產品說明書中加入“黑框警告”,只有其他治療溼疹的方法不能奏效時才能开具此藥。

英國藥品和保健產品監管機構也在2012年發文指出:他克莫司外用軟膏產品可能有“惡性腫瘤的風險,包括淋巴瘤和皮膚癌”,並明確指出他克莫司的允許用量標准爲0.03%和0.1%,其中低添加藥品只適用於2-16歲人群,且明令禁止給2歲以下兒童开具此類藥物處方。但此類藥品究竟是否致癌,目前在學界也尚有爭議,比如新近發表的分析結果就否認了他克莫司類成分會致癌[2]。
另外,Clin Exp Dermatol雜志2022發表的論文(Safety of tacrolimus 0.03% and 0.1% ointments in young children with atopic dermatitis: a 36-month follow-up study)指出,他克莫司可以作爲兒童特應性皮炎治療的一個選擇,可以用於2歲以下兒童,但其使用仍然應當受到限制。
在國內,復旦大學附屬華山醫院皮膚科等多家醫院都曾开展他克莫司在小兒特應性皮炎(AD)治療的探索,復旦大學附屬華山醫院副主任醫師馬英、陳連軍在研究成果《他克莫司軟膏在皮膚科的應用進展》中曾表示“總的來說,他克莫司外用是安全的、有效的[3]。”
資深護膚專家冰寒也指出,他克莫司類成分作爲一種免疫抑制劑,可以抑制免疫相關的一些炎症反應,例如紅斑、水腫等等,這樣就可能對於一些嬰兒溼疹、紅屁股、特應性皮炎之類的問題有緩解作用。
因此總結上述觀點,他克莫司類成分具有緩解嬰童溼疹、皮炎的效果,但在藥用產品中有嚴格的用量標准,且在“2歲以下兒童能否使用”“是否有致癌風險”這兩個問題上尚無統一結論。
進一步說,他克莫司即便作爲藥物也是病情嚴重時才能在醫囑下使用的處方藥,如果被違法添加到兒童化妝品中,在消費者不知情的情況下長期使用,其風險性不言而喻。
冰寒特別指出,有一些皮膚疾病與微生物感染相關(如脂溢性皮炎),免疫系統發生反應實際上是保護性、防御性的,如果不處理微生物,而是一味地抑制免疫系統,則反過來會進一步削弱自身防御,加重病情發展。“這在我的工作實踐中看到過實際的案例,但這一情況尚未引起關注。”
嬰童護膚品成質量問題“重災區”
令人感到蹊蹺的是,查看涉事公司中浩生物相關背景不難發現,它與此前備受關注的“大臉娃娃”面霜事件的始作俑者廣州恆瀾生物科技的有限公司(以下簡稱“恆瀾生物”)有着千絲萬縷的聯系。
國家企業信用信息公示系統顯示,兩家公司的注冊地完全一樣,且恆瀾生物股東何某某與原生產負責人莫某某均曾經擔任中浩生物公司法定代表人。

兩家公司也都在國藥監局備案了“紅色蝸牛嬰初霜”產品,兩個備案中的產品、外觀、功效基本一致,此前中恆瀾生物的備案已經被注銷,中浩生物的紅色蝸牛嬰初霜的備案也在7月13日被注銷。
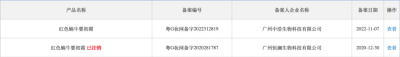


而恆瀾生物在兒童化妝品違規添加方面曾有過“前科”,曾在2021年因激素添加造成“大頭娃娃”事件而被處罰。
2021年1月,多名家長反饋嬰兒“戒之館”品牌產品後出現臉部腫大、多毛等“大臉娃娃”症狀,“戒之館”嬰親霜就是由廣州慕膚護膚品有限公司委托,廣州恆瀾生物科技有限公司生產。
2022年10月,廣東省藥品監督管理局曾因在兒童護膚產品添加激素類物質就對廣州恆瀾生物科技有限公司法定代表人吳某某、生產負責人莫某某作出處罰,兩人被終身禁止從事化妝品生產經營活動。
這是化妝品行業內第一個生產負責人被禁業的案例,也是生產負責人相關新規出台之後廣受關注的行業“第一罰”。
然而,官方監管機構的頂格處罰,似乎並沒有讓相關企業退回紅线之內,反而讓一些企業在違規添加之路上變得“更聰明”。
有業內人士指出,常規違規添加檢測主要集中在激素類物質上,新規之前無法測出非激素類的他克莫司,不在產品中添加激素而改爲藥用成分,可以說成功鑽了法規管理的漏洞。而且,將“無激素添加”作爲紅色蝸牛嬰初霜的核心賣點之一,打造安全的品牌認知,這種做法又極爲諷刺。
值得注意的是,違規添加問題或許只是嬰童膏霜類產品中的冰山一角,日常營銷中的虛假宣傳、妝藥模糊化,以及過分誇大“小金盾”,已經成爲同類產品的“常規手段”。
在電商平台上銷售的大量嬰童膏霜類產品打着“紅癢”、“紅疹”、“抑菌”等涉醫的療效,而實際銷售的產品爲國產普通化妝品,甚至有店鋪直接銷售“老款戒之館”產品。
2022年1月1日,《兒童化妝品監督管理規定》已正式施行,明確定義兒童化妝品是指適用於年齡在12歲以下(含12歲)兒童,具有清潔、保溼、爽身、防曬等功效的化妝品,要求兒童化妝品應當在銷售包裝展示面標注兒童化妝品標志“小金盾”,應當以“注意”或者“警告”作爲引導語,在銷售包裝可視面標注“應當在成人監護下使用”等警示用語。
值得一提的還有,不少門店將兒童護膚類產品的標志“小金盾”當作賣點,將其描述爲功效與安全性的保證。基於這種現象,國家藥品監督管理局曾明確表示,“小金盾”僅說明產品屬於兒童化妝品,並不代表該產品已經獲得監管部門審批或者質量安全得到認證。
好在隨着國家層面和社會領域的科普,大衆消費者相關認知在逐漸提升。兒童用妝安全不可小視,當全社會對嬰童護理類產品的違法行爲重視程度變得更高、容忍程度降到極低,不法企業鑽空子的可能性也變得越來越小。
放眼全球日化領域,強生“爽身粉”官司持續時間之久,判罰力度之大,備受矚目。
反觀此次事件中,國家藥品監督管理局的迅速反應,給出相應的檢測辦法,各地職能部門已經在統一部署之下對此事進行核查,監管的效率之高已有目共睹。
然而,肅清毒瘤,正本清源,對於違法行爲的整治依舊任重道遠,本次事件無疑讓全社會對嬰童護膚品的安全問題再次繃緊了神經。
“絕不能姑息!他們是拖累國內品牌的‘害群之馬’,加深了消費者的安全恐慌。”有資深行業人士直呼,這種行爲在坑害消費者的同時,也抹黑了整個行業,理應得到最嚴厲的懲罰。
[1]蘇澤軒,於立新,黃傑夫主編.現代移植學[M].北京: 人民衛生出版社.1988:117∙
[2]Devasenapathy N, Chu A, Wong M, et al. Cancer risk with topical calcineurin inhibitors, pimecrolimus and tacrolimus, for atopic dermatitis: a systematic review and meta-analysis[J]. The Lancet Child & Adolescent Health, 2023.)。
[3]馬英,陳連軍.他克莫司軟膏在皮膚科的應用進展 上海醫藥 2010年 第31卷 第4期
END
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:大量注銷!嬰兒霜“抗生素事件”已被立案
地址:https://www.breakthing.com/post/78444.html







