恩沃利單抗獲批兩周給藥方案,大幅提高用藥便捷性
2年前

恩沃利單抗獲批兩周給藥方案,大幅提高用藥便捷性
8月19日,康寧傑瑞生物制藥宣布,其自研的全球首款皮下注射PD-L1抑制劑恩維達(恩沃利單抗注射液)新增“300mg每兩周給藥一次”的用法用量方案,獲國家藥品監督管理局(NMPA)批准。 本次新增的劑量用法方案,與此前恩維達的推薦劑量及用法“150mg每周給藥一次”相比,有着相似的藥代謝動力學、安全性和有效性特徵。此次方案的獲批,可以在保證恩維達臨牀效果的前提下,發揮更大臨牀應用意義。對於醫生來說,用藥方案更加靈活,可根據患者實際情況選擇單周給藥抑或雙周給藥;對於患者而言,藥物的依從性有望得到提升,可直接減少就醫頻率,爲患者帶來方便,並減少醫療資源的佔用。 恩維達是康寧傑瑞自主研發的PD-L1單域抗體Fc融合蛋白,是全球第一個且目前唯一獲批上市的皮下注射PD-(L)1抗體。基於其獨特設計,在安全性、便利性和依從性方面具有優勢,患者無需進行靜脈滴注,同時具有較低的醫療成本。
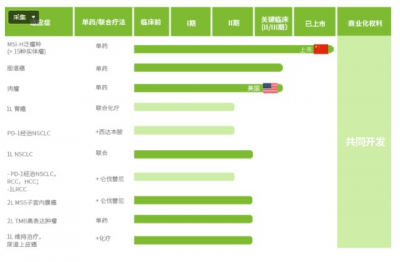 恩維達的研究進展(來源:康寧傑瑞官網)
恩維達的研究進展(來源:康寧傑瑞官網)
恩維達目前正在中國、美國和日本开展多個腫瘤適應症的臨牀研究,多個適應症已進入注冊/Ⅲ期臨牀。恩維達已被美國FDA授予晚期膽道癌孤兒藥資格、軟組織肉瘤孤兒藥資格。2021年11月,恩維達在中國獲批上市,適用於不可切除或轉移性微衛星高度不穩定(MSI-H)或錯配修復基因缺陷型(dMMR)的成人晚期實體瘤患者的治療。 恩維達由康寧傑瑞自主研發,2016年起與思路迪醫藥共同开發,2020年3月30日,康寧傑瑞、思路迪醫藥、先聲藥業三方達成战略合作,康寧傑瑞作爲原研方負責生產和質量,思路迪醫藥負責腫瘤領域的臨牀开發,先聲藥業負責產品在中國大陸的獨家商業推廣。
追加內容
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:恩沃利單抗獲批兩周給藥方案,大幅提高用藥便捷性
地址:https://www.breakthing.com/post/15179.html







