挑战阿柏西普!信達生物CR1/VEGFR融合蛋白啓動III期研究
1年前

挑战阿柏西普!信達生物CR1/VEGFR融合蛋白啓動III期研究
 7月28日,信達生物在藥物臨牀試驗登記與信息公示平台登記了一項III期臨牀試驗,旨在評估IBI302(8mg)對比阿柏西普(2mg)治療新生血管性年齡相關性黃斑變性(nAMD)的有效性和安全性。
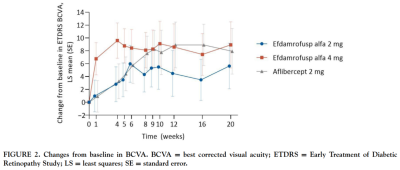
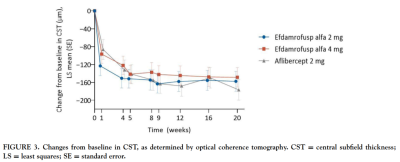
7月28日,信達生物在藥物臨牀試驗登記與信息公示平台登記了一項III期臨牀試驗,旨在評估IBI302(8mg)對比阿柏西普(2mg)治療新生血管性年齡相關性黃斑變性(nAMD)的有效性和安全性。  IBI302(efdamrofusp alfa)是信達生物在2012年自圓祥生命科技(前稱:ProtevoBio)引進的一款同時靶向補體受體1(CR1)和血管內皮生長因子受體(VEGFR)的雙特異性融合蛋白,該筆交易首付款爲25萬美元,總金額爲450萬美元。該產品也是全球首款CR1/VEGFR雙特異性融合蛋白。 IBI302的N末端可與VEGF家族結合並阻斷其介導的信號通路,從而抑制血管上皮細胞增殖和血管生成,降低血管通透性和減少滲漏;IBI302的C末端可以特異性結合C3b和C4b並抑制二者介導的補體激活經典途徑和補體激活替代途徑,減少補體介導的炎症反應。通過以上兩種機制,IBI302可以實現治療和控制nAMD的目的。 此前,信達生物已完成兩項IBI302治療nAMD的I期臨牀研究。結果表明,IBI302具有良好的安全性和耐受性,患者接受治療後視力明顯改善且視網膜水腫也有所減少。
IBI302(efdamrofusp alfa)是信達生物在2012年自圓祥生命科技(前稱:ProtevoBio)引進的一款同時靶向補體受體1(CR1)和血管內皮生長因子受體(VEGFR)的雙特異性融合蛋白,該筆交易首付款爲25萬美元,總金額爲450萬美元。該產品也是全球首款CR1/VEGFR雙特異性融合蛋白。 IBI302的N末端可與VEGF家族結合並阻斷其介導的信號通路,從而抑制血管上皮細胞增殖和血管生成,降低血管通透性和減少滲漏;IBI302的C末端可以特異性結合C3b和C4b並抑制二者介導的補體激活經典途徑和補體激活替代途徑,減少補體介導的炎症反應。通過以上兩種機制,IBI302可以實現治療和控制nAMD的目的。 此前,信達生物已完成兩項IBI302治療nAMD的I期臨牀研究。結果表明,IBI302具有良好的安全性和耐受性,患者接受治療後視力明顯改善且視網膜水腫也有所減少。
推薦閱讀
中國創新藥需要“頭鐵”玩家羅氏2023H1:眼科雙抗破10億美元,中國區收入超30億美元
Copyright 2023 PHARMCUBE. All Rights Reserved.
歡迎轉發分享及合理引用,引用時請在顯要位置標明文章來源;如需轉載,請給微信公衆號後台留言或發送消息,並注明公衆號名稱及ID。
免責申明:本微信文章中的信息僅供一般參考之用,不可直接作爲決策內容,醫藥魔方不對任何主體因使用本文內容而導致的任何損失承擔責任。
追加內容
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:挑战阿柏西普!信達生物CR1/VEGFR融合蛋白啓動III期研究
地址:https://www.breakthing.com/post/83684.html







