

據藥融雲數據庫統計,7月1日至31日期間,CDE共承辦294條新注冊分類仿制藥申報受理號和91條一致性評價補充申請,涉及藥企超三百家。
其中,浙江賽默制藥申報品種多達10個,宜昌人福、華仁藥業、石家莊四藥、辰欣藥業等企業也持續發力,陸續遞交4-5個品種的仿制上市申請。
與此同時,7月共有131品種過評(環比下降19%),科倫收獲最多,共有5品種過評;宜昌人福、青峰醫藥等均斬獲4款藥品過評。
一致性評價申報情況
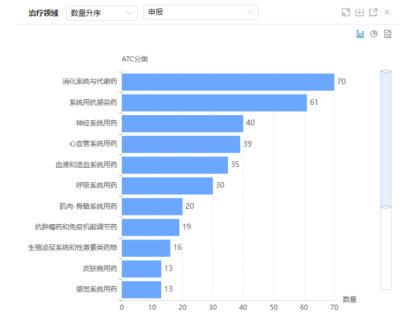
7月期間,CDE共承辦294條新注冊分類仿制藥申報受理號和91條一致性評價補充申請,涉及藥企超三百家。申報品種最集中的領域是消化系統與代謝藥領域,其次爲系統用抗感染藥。
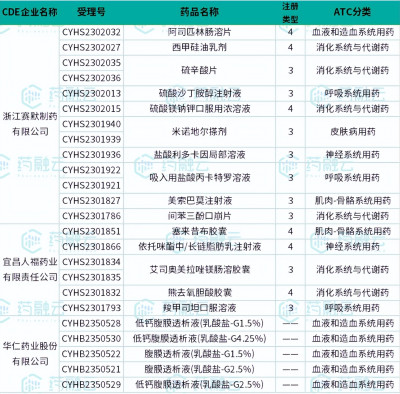
從各企業申報情況來看,浙江賽默制藥有限公司申報最多,共遞交了10個品種的仿制上市申請或一致性評價補充申請。其次爲宜昌人福、$華仁藥業(SZ300110)$、石家莊四藥、$辰欣藥業(SH603367)$等藥企,均申報了4-5個仿制藥品種上市。
總體看來,申報數量排名前列的企業均爲國內產品豐富的制藥大廠,大型企業優勢明顯。
申報品種數≥5的企業
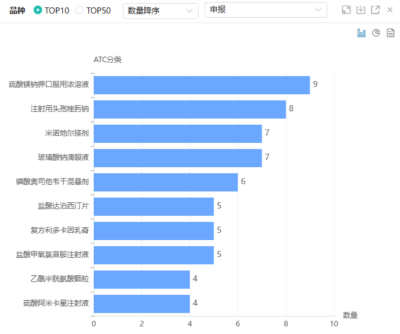
從受理品種來看,硫酸鎂鈉鉀口服用濃溶液、注射用頭孢唑肟鈉等品種的相關申報企業數最多。前者申報企業有浙江恆研醫藥/浙江賽默制藥、河北合渡藥業/樂聲藥業、南京海鯨藥業、長春瀾江醫藥/湖南九典制藥和麗珠集團/天大藥業;後者申報企業有山東如至生物醫藥/沈陽三九藥業、海南仲悅醫療/福建省福抗藥業、陝西東科制藥/上海欣峰制藥、成都天之翼尚品醫藥/山東魯抗醫藥等。
7月新增過評情況
7月,共有131個品種(217品規)通過/視同通過一致性評價,相較6月環比下降19%,涉及130家企業。
從品種來看,磷酸西格列汀片過評企業最多,達4家;注射用哌拉西林鈉他唑巴坦鈉、非布司他片、地氯雷他定口服溶液、鹽酸莫西沙星滴眼液、磷酸奧司他韋膠囊等均新增3家藥企過評。
從企業來看,科倫(5)、人福(4)、迪賽諾醫藥(4)、青峰藥業(4)、石家莊四藥(3)、四川匯宇制藥(3)等收獲較多。
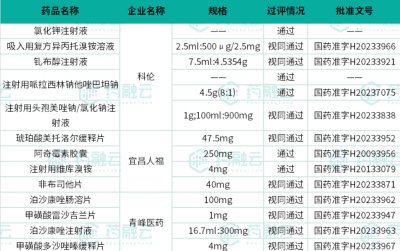
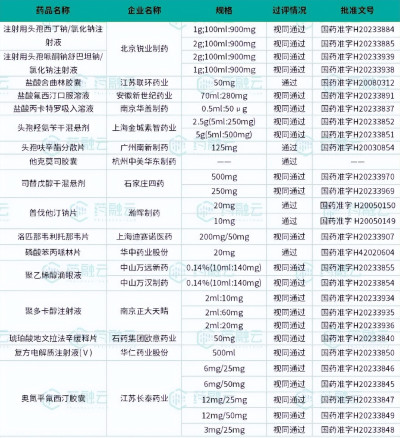
首家過評品種方面,本月共有17個品種迎來首家過評,涉及南京正大天晴、石藥歐意、杭州中美華東制藥等多家藥企。
7月首家過評品種
<END>
本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:7月仿制藥战況:131品種過評,17款首家,科倫、人福、石四藥…
地址:https://www.breakthing.com/post/84464.html







