
1月9日,CDE官網顯示,禮來的donanemab注射液擬納入突破性療法,擬定適應症爲早期症狀性阿爾茨海默病(AD),包括阿爾茨海默病所致的輕度認知障礙以及輕度阿爾茨海默病。
Donanemab是一款靶向pGlu3-A的抗體,這種焦谷氨酸修飾的amyloid beta也叫A (p3-42)、pE3-A、N3pG。pGlu3-A沒有生理功能,存在於阿爾茨海默病澱粉樣蛋白沉積物中。
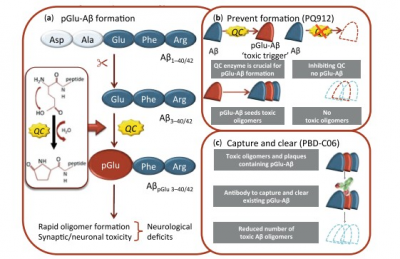
來源:nature
2021年6月,基於其II期臨牀數據,FDA授予該適應症的突破性療法認定。目前,禮來已完成該產品的滾動上市申請,FDA預計今年2月做出審批決定。
2022年12月,禮來公布了donanemab用於早期AD的III期TRAILblazer-ALZ 4研究的積極數據,該研究旨在評估donanemab vs aducanumab對早期AD患者澱粉樣蛋白斑塊清除的影響。結果顯示,治療6個月後,donanemab組有37.9%(25/66)患者達到澱粉樣蛋白斑塊完全清除(定義爲澱粉樣蛋白等級<24.1CL),而aducanumab組患者比例爲1.6%(1/64)。在中間tau亞群中,分別有38.5%(10/26)和3.8%(1/26)的患者澱粉樣蛋白斑塊完全清除。
在一個關鍵次要終點上,接受donanemab和aducanumab治療後,患者腦澱粉樣蛋白水平較基线分別降低了65.2%和17%。此外,與基线相比,donanemab治療組也顯著降低了血漿P-tau217水平。
參考資料: [1]Developing a new generation of Alzheimer’s disease treatments. nature.comCopyright 2023 PHARMCUBE. All Rights Reserved.
歡迎轉發分享及合理引用,引用時請在顯要位置標明文章來源;如需轉載,請給微信公衆號後台留言或發送消息,並注明公衆號名稱及ID。
免責申明:本微信文章中的信息僅供一般參考之用,不可直接作爲決策內容,醫藥魔方不對任何主體因使用本文內容而導致的任何損失承擔責任。

本文作者可以追加內容哦 !
鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播信息之目的,不構成任何投資建議,如有侵權行為,請第一時間聯絡我們修改或刪除,多謝。
標題:禮來阿爾茨海默病新藥donanemab注射液擬納入突破性療法
地址:https://www.breakthing.com/post/39568.html







